丙型肝炎由丙型肝炎病毒(HCV)感染所致,主要由血液/体液传播。据世界卫生组织估计,全球有1.7亿人感染HCV。在我国健康人群抗HCV阳性率为0.7%~3.1%,约3800万人。由于病毒生物学特点和宿主免疫功能等多方面因素,机体免疫往往难以有效清除病毒,致使约50%~80%HCV感染者发展为慢性肝炎,其中20%~30%将发展成肝硬化。肝硬化患者中每年有1%~4%发展成为肝细胞癌症。
HCV是一种RNA病毒。HCV RNA大约有9500~10000bp组成,5'和3'非编码区(NCR)分别有319~341bp,和27~55bp,含有几个顺向和反向重复序列,可能与基因复制有关。在5'非编码区下游紧接一开放的阅读框(ORF),其中基因组排列顺序为5'-C-E1-E2-p7-NS2-NS3-NS4-NS5-3',能编码一长3014个氨基酸的多聚蛋白前体,可经宿主细胞和病毒自身蛋白酶作用后,裂解成各自独立病毒蛋白,即三种结构蛋白,为分子量19KD的核衣壳蛋白(或称核心蛋白,C)和33KD(E1),72Kd(E2/NS1)的糖蛋白,及四种分子量为23KD、52KD、60KD、116KD的非结构蛋白分别与NS2、NS3、NS4、NS5相对应。由于GP72正好与瘟病毒表面蛋白或黄病毒第一个非结构蛋白(NS1)相对应,故将GP72的基因标记称谓E2/NS1。E1和E2/NS1糖蛋白能产生抗HCV的中和作用。NS2和NS4的功能还不清楚,发现与细胞膜紧密结合在一起。NS3蛋白具有螺旋酶活性,参与解旋HCV-RNA分子,以协助RNA复制,NS5有依赖于RNA的聚合酶活性,参与HCV基因组复制。
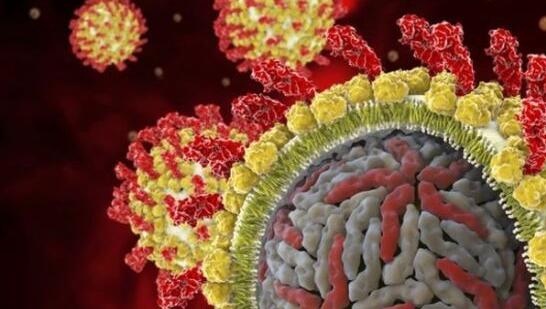
丙型肝炎病毒(HCV)是一种小型的包膜病毒:单股正链RNA病毒,包被在蛋白衣壳中,含有两种糖蛋白的脂质双层包膜包绕着这种蛋白衣壳,而且包膜上有剌突。急性HCV感染能够导致肝炎,但是这种病毒通常是以在肝脏中慢性感染的形式持续存在,并且这种持续存在能够导致肝脏炎症,以及最终导致肝细胞癌。HCV如何破坏肝细胞将它们变成病毒制造工厂仍然是个谜。
在一项新的研究中,来自法国里昂的Romain Parent和他的合作者发现一种小分子量分泌蛋白,Netrin-1,密切地参与HCV的生命周期。他们报道HCV增加肝细胞中的Netrin-1表达,接着,Netrin-1增加病毒RNA基因组数量和产生的病毒颗粒的传染性。更为重要的是,他们提供证据证实Netrin-1也促进HCV病毒被未感染的肝细胞摄取,这很可能是通过阻断表皮生长因子受体(EGFR)内化因而增加这种用于病毒摄取的辅因子在肝细胞表面上的数量来实现的。相关研究结果于2016年3月31日发表在PLoS Biology期刊上,论文标题为“Epidermal Growth Factor Receptor-Dependent Mutual Amplification between Netrin-1 and the Hepatitis C Virus”。
HCV主要在肝脏的肝细胞(hepatocyte, 也译作肝实质细胞)中进行复制。它通过与几种细胞表面蛋白的复杂相互作用而侵入这些肝细胞,并在细胞内膜上进行复制,特别是在内质网膜上。研究人员之所以研究Netrin-1在HCV感染中发挥的可能性作用,是因为之前的研究已证实它参与几种类型的癌症以及与癌症相关联的炎症性疾病。
研究人员首先研究从HCV患者体内获取的肝脏活组织样品中的Netrin-1 mRNA数量,然后将这种数量与来自未感染HCV的病人的类似样品进行比较。他们发现在被HCV感染的样品中Netrin-1 mRNA数量显著增加,增加了23倍,对HCV感染病人进行抗病毒药物治疗能够逆转这种增加。类似地,HCV感染原代人肝细胞和在体外培养的肝细胞系会导致这些细胞中的Netrin-1 mRNA数量大量增加,因而也会导致新翻译的Netrin-1蛋白数量显著增加。
已知Netrin-1 mRNA结合到La相关蛋白LARP1上,但是这种相互作用的功能重要性是不清楚的。研究人员发现LARP1也在促进Netrin-1翻译的内质网膜上特异性地与非结构性HCV蛋白NS5A发生相互作用。再者,在过量表达和基因敲除研究中,Netrin-1水平直接与被HCV感染的肝细胞中HCV RNA数量和所产生的病毒颗粒的传染性相关联,而且Netrin-1很可能是通过直接结合到HCV病毒颗粒上来实现的。因此,研究人员作出结论,HCV感染促进Netrin-1产生,接着,Netrin-1促进HCV产生。
但是这不是Netrin-1对HCV生命周期的唯一影响。研究人员也提供证据证实表达的Netrin-1通过阻止EGFR内化,增加肝细胞表面上的EGFR蛋白水平---以及活化的(磷酸化的)EGFR水平,而且这似乎促进HCV病毒侵入肝细胞。
(
将来商城www.jonln.com)